Studies on enantiospecific synthesis, structural analysis, and neuronal activity of an artificial glutamate analog TKM-38
IKM–159はダイシハーベインとカイニン酸の特徴を併せ持つAMPA受容体リガンドとして当研究室で開発された人工グルタミン酸で、マウスによるin vivo活性評価の結果から、その2R体が神経活性を担うことが判明している。当研究室では、昨年度までに新規八員環アナログ (TKM–38) の両鏡像体の合成を達成した。これらの化合物は合成中間体を含め結晶性に乏しく、X線回折による構造解析が適用できなかったため、NMR (NOESY) と配座計算 (CONFLEX) によってその立体化学は推定されるにとどまっていた。
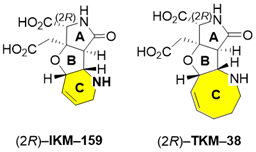
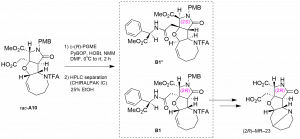
TKM–38はマウスによる評価の結果2S体、2R体ともに不活性であることが判明していたが、構造活性相関の観点から、より信頼性の高い手法でその構造を確定する必要があった。そこで本研究では、PGME法を用いてTKM–38の絶対立体化学を決定することを目的とした。PGMEはキラルなアミンで、それが含むPh基による遮蔽効果により両鏡像異性体で1H NMRの化学シフト値に差が生じることを利用してカルボン酸の絶対立体化学を決定することに用いられる。本研究ではカルボン酸rac–A10にPGMEを縮合させ、得られたジアステレオマー混合物をキラルカラムを用いたHPLCにより分離した。それぞれの1H NMRを測定し、二次元NMRを用いて帰属した。化学シフト値の差を求めて構造式に当てはめると、正負の分布が分子構造の左右ではっきりとわかれ、それらの立体化学を決定することができた。2R体と判断されたジアステレオマーを順次脱保護し、最終加水分解によりTKM–38を得ようとしたが、従来の方法であるKOHを用いたアルカリ加水分解では目的物は得られなかった。そこで塩酸を用いた酸加水分解を試みたところ、TKM–38とは異なる化合物が得られた。我々はこれを (2R)–MR–23と名付けた。この結果を受けて、過去に合成したメンチルエステル前駆体の両ジアステレオマーについても同様の条件で反応を行ないHPLCにおける溶出時間を比較したところ、先行研究において 2R体と判断されていたものから生じた生成物と (2R)–MR–23が同一であることがわかった。このことから、先行研究における構造解析が正しかったことを示すことができた。我々はMR–23は5/5/5/5員環からなる四環性の構造をとると推定しており、これをベースに合成を進めれば五員環アナログの合成ルートに繋がる可能性がある。 五員環アナログはこれまでにない強い神経活性を持っている可能性があると示唆されている。そのため、MR–23の構造を明らかにし、そこから五員環アナログへ導くため、現在はMR–23の大量合成を試みている。
参考文献
- Tsukamoto, S., Master Thesis 2020, Yokohama City University.
- Kusumi, T.; Yabuuchi, T., J. Org. Chem. 2000, 65, 397-404.


